Хормони на задстомашната жлеза.
Ендокринният панкреас секретира два главни пептидни хормона, инсулин и глюкагон, чиито функции са да регулират глюкозния, мастнокиселинния и аминокиселинния метаболизъм. Секретират се също соматостатин и панкреатичен полипептид, но техните функции не са достатъчно добре проучени.

Ендокринните клетки на панкреаса са подредени в пространства, наречени острови на Лангерханс – те заемат 1-2% от панкреатичната маса. Има около 1 милион острови на Лангерханс, които са струпани предимно в опашната част на жлезата. Островите съдържат четири клетъчни типа. А-клетките са 20% от ендокринните клетки и секретират хормона глюкагон. B-клетките са 65% от ендокринните клетки и секретират хормона инсулин. D-клетките са 10% от клетките и секретират хормона соматостатин, а F-клетките са 5% и секретират панкреатичен полипептид.
Хормоните на панкреаса осъществяват паракринни взаимодействия помежду си.
Инсулин – физиологични действия
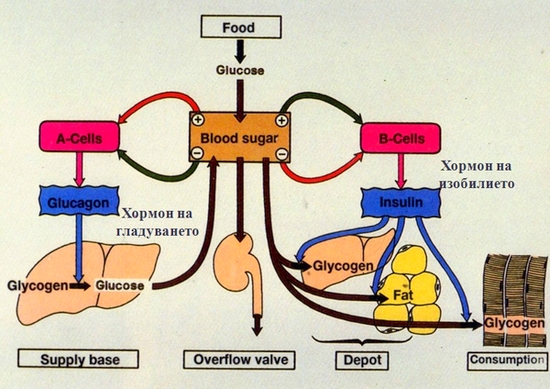
Инсулинът е познат като „хормон на изобилието”. Когато приемът на хранителни вещества надвиши изискванията на тялото, инсулинът осигурява излишъкът на вещества да се складира като гликоген в черния дроб, като масти в мастната тъкан и като протеини в мускулите – това негово действие е анаболно. Складираните под действие на инсулина хранителни запаси са на разположение по време на периоди на гладуване или постене, за да се поддържа глюкозна доставка към мозъка и други жизнено важни органи.

Основните прицелни органи и тъкани за действията на инсулина са черният дроб, мускулите и мастната тъкан. Инсулинът засилва транспортът на глюкоза в прицелните клетки, които притежават рецептори за инсулин (влакната на напречно набраздените мускули, влакната на миокарда, гладкомускулните влакна на матката, клетките на мастната тъкан). Така глюкозната концентрация в кръвта се понижава и се ограничава повишаването на кръвната захар след консумиране на въглехидрати.
Инсулинът не повлиява глюкозния транспорт в мозъка – глюкозата навлиза в мозъчните клетки чрез проста дифузия. Реабсорбцията на глюкоза в бъбречните каналчета и в тънкото черво се извършва чрез вторично активен транспорт, който също не зависи от инсулина.
Инсулинът подпомага гликогеносинтезата в черния дроб и мускулите – формирането на гликоген от глюкоза. Едновременно с това инсулинът инхибира гликогенолизата – гликогеновото разпадане.
Инсулинът инхибира глюконеогенезата – формирането на глюкоза от аминокиселини, мастни киселини и глицерол.
Затова пък инсулинът увеличава навлизането на аминокиселините в мускулите и протиновата синтеза и инхибира протеиновата деградация. По такъв начин инсулина подпомага растежа и възстановяването след боледуване или гладуване.
Инсулинът стимулира депозирането на масти в мастната тъкан и инхибира липолизата и формирането на кетокиселини в черния дроб.
Фактори, които стимулират секрецията на инсулин

Повишаването на глюкозната концентрация в кръвта бързо стимулира секрецията на инсулин от В-клетките. Повишената концентрация на аминокиселините и мастните киселини също стимулира инсулиновата секреция. Глюкагонът причинява секреция на инсулин.
При вагусова стимулация, ацетилхолинът стимулира секрецията на инсулин в кръвта.
Фактори, които инхибират секрецията на инсулин
Инсулиновата секреция се преустановява, когато концентрацията на глюкозата в плазмата е под 2.5 mmol/l (хипогликемия). На същата основа при гладуване и физическо натоварване инсулиновата секреция се потиска.
Захарен диабет или инсулин-зависим диабетес мелитус (Тип 1) е заболяване, което се проявява, когато В-клетките в панкреаса не секретират достатъчно количество инсулин. Пациенти със захарен диабет имат сериозни метаболитни нарушения: въглехидратната, мастната и белтъчната обмяна са нарушени. В резултат тези нарушения глюкозната концентрация в кръвта се увеличава (хипергликемия) – особено след нахранване. Увеличават се концентрациите на мастните киселини и кетокиселините в кръвта поради увеличено разграждане на мастите (липолиза). Болните губят мастна тъкан и телесна маса (катаболно състояние). Изчерпването на белтъците води до намалена резистентност към инфекции, а богатите на глюкоза телесни течности са добра среда за развитие на бактерии. Силно изразената хипергликемия при недобре лекуван диабет води до увеличена филтрация на глюкоза в бъбречните гломерули и поява на глюкоза в урината (глюкозурия). Последствие от глюкозурията е полиурията, която се дължи на осмотична диуреза – обемът на отделената урина се увеличава поради задържане на вода в бъбречните тубули от нереабсорбираната глюкоза. Полиурията води до дехидратация (обезводняване) на организма на болните и затова те изпитват жажда и приемат повече вода.
Увеличената концентрация на кетокиселините в кръвта, която е последствие от нарушения мастен метаболизъм, предизвиква метаболитна ацидоза. Ацидозата и дехидратацията заедно водят до потискане на съзнанието и кома.
Глюкагон

В повечето аспекти глюкагонът е “огледално отражение” на инсулина. Докато инсулинът е “хормон на изобилието”, глюкагонът е “хормон на гладуването”. Глюкагонът спомага за мобилизацията и използването на метаболитните горива, а не за тяхното складиране. Глюкагонът стимулира гликогенолиза и глюконеогенеза в черния дроб и така предизвиква покачване на нивото на кръвната захар. Глюкагонът предизвиква липолиза в мастните депа и повишаване на концентрацията на мастни киселини и кетокиселини в кръвта.
Секрецията на глюкагон се стимулира от хипогликемия.